세포 노화 전염 핵심 단백질 HMGB1 첫 입증
세포 하나가 늙었을 뿐인데 왜 온몸이 함께 늙는지를 설명하는 과학적 해답이 세계 최초로 국내 연구진에 의해 밝혀졌다.
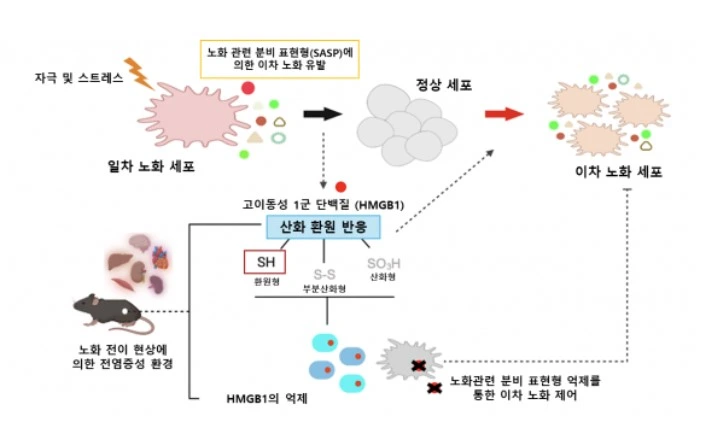
고려대학교 의과대학 융합의학교실 전옥희 교수 연구팀은 세포 노화를 주변 조직으로 확산시키는 핵심 단백질 ‘HMGB1(High Mobility Group Box 1)’의 역할을 규명했다고 21일 밝혔다.
연구에 따르면, 노화된 세포는 단순히 기능 저하에 머무르지 않고 ‘HMGB1’ 단백질을 분비해 혈액을 타고 퍼뜨린다.
이 단백질은 다른 정상 세포에 염증 반응을 유도하고 ‘노화 유도 신호’를 전달함으로써 주변 세포마저 늙게 만든다.
이는 근육을 포함한 전신 장기의 재생 능력과 기능 저하로 이어진다.
이 같은 현상은 ‘노화-연관 분비 표현형(SASP, Senescence-Associated Secretory Phenotype)’으로 알려져 있다.
나이가 들수록 노화 세포가 축적되며, 이들이 내뿜는 신호로 인해 인접한 세포들까지 연쇄적으로 노화되면서 몸 전체가 늙는 것이다.
전 교수 연구팀은 실험을 통해 HMGB1 단백질의 활성을 억제하면 노화의 확산을 막을 수 있다는 사실도 밝혀냈다.
쥐를 대상으로 해당 단백질을 차단하는 항체를 투여하자 전신 염증 반응이 줄고, 손상된 근육 조직의 회복 속도 또한 빨라졌다.
특히 HMGB1이 세포에 신호를 전달할 때 사용하는 수용체 ‘RAGE’를 차단했을 때도 유사한 효과가 나타났다.
이번 연구는 노화가 특정 세포에 머무르지 않고 혈류를 통해 전신으로 확산되는 ‘노화 전이’의 분자 생물학적 기전을 최초로 입증했다는 데 큰 의의가 있다.
연구팀은 이를 통해 노화성 질환이나 만성 염증성 질환의 새로운 치료 전략 수립에 기반을 제공할 수 있다고 기대하고 있다.
전옥희 교수는 “노화가 특정 세포나 조직에만 머무는 것이 아니라, 혈액을 통해 전신으로 확산하는 ‘노화 전이’ 현상을 설명할 수 있는 분자적 기전을 밝힌 것”이라며 “향후 노화 관련 질환을 치료할 수 있는 새로운 전략을 제시했다는 점에서 의미가 크다”고 말했다.
이번 연구는 미국 UC버클리와 터프츠대학교와의 공동연구로 진행됐으며, 내분비대사 분야의 국제학술지 Metabolism: Clinical and Experimental에 최근 게재됐다.
배동현 (grace8366@sabanamedia.com) 기사제보






